Bạn thích hóa, bạn đã học hóa thì chức bạn không thể không biết tới công thức tính thể tích khí ở ddktc, một trong những công thức cự kì ngắn gọn và vi diệu. Nó tưởng chừng như đề bài cho thiếu nhưng lại luôn phải biết hằng số 22,4.
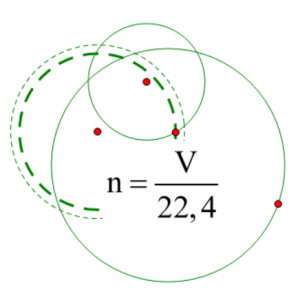
Công thức tính thể tích: $n = \frac{v}{{22,4}}$
- n là số mol
- v là thể tích của chất khí ở điều kiện tiêu chuẩn (lít)
Tới đây có bạn sẽ hỏi điều kiện tiêu chuẩn là gì?
Trả lời: Khi đo 1 đại lượng vật lý trong phòng thí nghiệm người ta quan tâm tới nhiệt độ và áp suất. Nếu nhiệt độ là 00C (hay 273,15 độ K) và áp suất là 1 atm (hay 100 kPa) thì => nhiệt độ tiêu chuẩn và áp suất tiêu chuẩn => Gọi là điều kiện tiêu chuẩn.
Ví dụ 1. Người ta điều chế N2 trong phòng thí nghiệm theo phản ứng NH4NO3 → N2 + 2H2O. Khí N2 thu được ở điều kiện tiêu chuẩn là 22,4 lít. Hãy tìm
a) số mol khí N2 thu được.
b) Khối lượng NH4NO3.
Hướng dẫn giải
Theo công thức tính thể tích khí ở đktc thì $n = \frac{v}{{22,4}} = \frac{{22,4}}{{22,4}} = 1\left( {mol} \right)$
a) Số mol khí N2 thu được n = 1 mol
b) Theo phản ứng thì số mol NH4NO3 = số mol khí N2.
Khối lượng NH4NO3: $m = n.{A_{N{H_4}N{O_3}}}$$ = 1.\left( {7 + 1.4 + 7 + 8.3} \right)$$ = 42\left( {g} \right)$
Ví dụ 2. Thả miếng kém vào dung dịch axit sunfuric thì thấy khí H2 bay nên. Người ta đo được lượng khí thu được ở điều kiện tiêu chuẩn là V = 11,2 lít. Hãy
a) Viết phương trình phản ứng
b) Tính khối lượng chất tan để thu được lượng khí trên
c) Trong thí nghiệm, người ta chỉ thu được 30% lượng khí H2 bay nên so với khí thực sinh ra từ phản ứng. Hỏi khối lượng chất tam đem làm phản ứng là bao nhiêu?
Hướng dẫn giải
a) Theo đề bài, ta có phản ứng: Zn + H2SO4 → ZnSO4 + H2↑
b) Vì chất khid được đo ở đktc nên số mol thu được được $n = \frac{v}{{22,4}} = \frac{{11,2}}{{22,4}} = 0,5\left( {mol} \right)$
Theo phản ứng nZn = nH2 = 0,5 (mol) => mZn = nZn.AZn = 0,5.65 = 32,5(g)
c) Thể tích V = 11,2 lít chỉ chiếm 30% lượng khí thực => số thể tích thực thu được là V’ = 11,2 : 30% = $\frac{{112}}{3}$ lít
Số mol khí thu được là $n = \frac{{V’}}{{22,4}}$$ = \frac{{\frac{{112}}{3}}}{{22,4}}$$ = \frac{5}{3}\left( {mol} \right)$
Khối lượng Zn đem tham gia phản ứng: m’ = n’.A = $\frac{5}{3}.65 = 108,333\left( g \right)$
Tài liệu thầy Hồ Thức Thuận: LINK TẢI ĐỀ – LINK TẢI ĐÁP ÁN